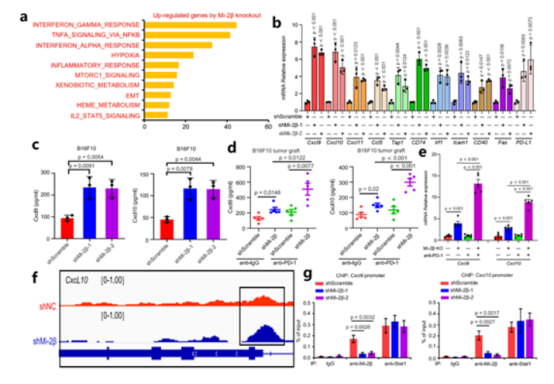
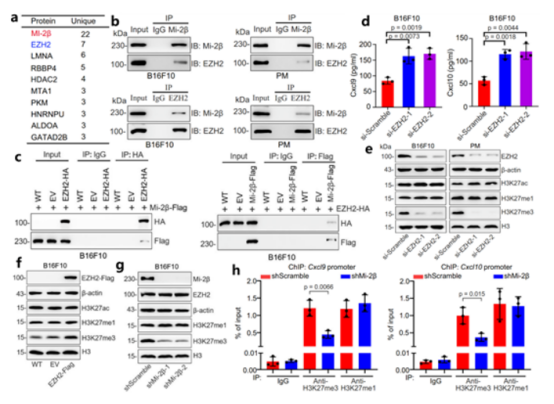
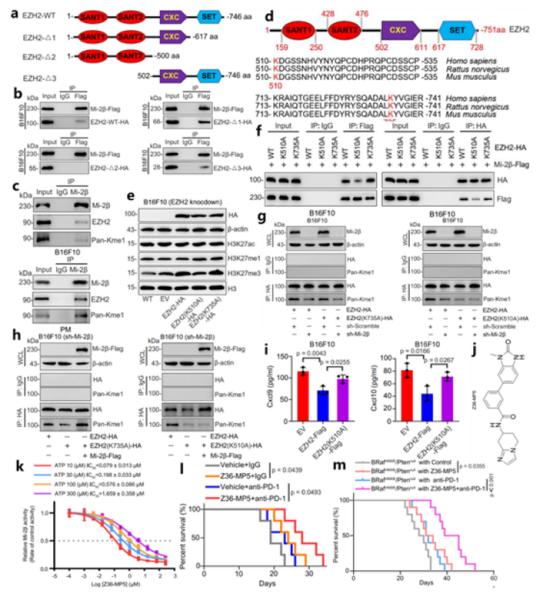
2024年3月,南昌大学教育部实体肿瘤分子靶向医药基础研究创新中心、浙江大学医学院附属第二医院崔儒涛团队在Nature Communications杂志上,发表“Mi-2β promotes immune evasion in melanoma by activating EZH2 methylation”的研究文章。体内、外实验显示Mi-2β缺失诱导黑色素瘤细胞对免疫治疗的应答。机制上,Mi-2β与EZH2结合,促进EZH2 K510甲基化,进而激活H3K27的三甲基化,抑制IFN-γ刺激基因(ISGs)的转录。开发了针对Mi-2β的靶向抑制剂Z36-MP5,在耐药黑色素瘤模型中诱导对免疫检查点抑制剂的响应。 Highlights如下: 1)Mi-2β的低表达与CD8+ T细胞浸润的富集相关、与T细胞介导的杀伤有关。 2)Mi-2β缺失诱导黑色素瘤细胞对免疫治疗的应答,上调IFN-γ信号。 3)机制上,Mi-2β控制ISGs的可及性,与EZH2结合,促进EZH2 K510甲基化,进而激活H3K27的三甲基化,抑制ISGs的转录。 4)开发一种靶向Mi-2β的抑制剂,Z36-MP5,可以降低Mi -2β ATP酶活性并重新激活ISG转录。 临床相关性: Mi-2β与CD8A和CD8B表达呈负相关。在CD8+ T细胞高浸润的黑色素瘤患者中,Mi-2β低表达与生存获益显著正相关。 功能研究: Mi-2β沉默显著诱导黑色素瘤细胞对T细胞攻击的响应;诱导免疫健全、BRafV600E/Ptennull小鼠模型免疫治疗应答,抑制肿瘤生长、延长小鼠在抗PD-1治疗后生存期。 机制研究: 为了确定Mi-2β如何影响黑色素瘤的免疫反应,进行微阵列分析。富集分析发现,Mi-2β敲除后,IFN-γ信号通路被激活(图1a),IFN-γ应答基因和抗原呈递基因上调(图1b)。IFN-γ在免疫治疗应答中起关键作用。Mi-2β沉默和抗PD-1治疗后Cxcl9和Cxcl10上调(图1c-e)。研究表明Mi-2β富集于基因组转录起始位点,在转录抑制中起重要作用。为了研究Mi-2β抑制IFN-γ信号的分子机制,进行ATAC-seq(染色质可及性),发现基因座内ATAC-seq峰的变化与IFN-γ信号相关(图1f)。随后,ChIP分析结果显示Mi-2β与Cxcl9和Cxcl10的启动子结合(图1g)。表明,Mi-2β的缺失重塑染色质的可及性,促进导致其转录激活的ISG调控区域的暴露。 图1 缺失Mi-2β通过促进染色质重塑促进干扰素刺激基因的转录 进一步研究Mi-2β调控ISGs表达的机制。IP-MS分析,EZH2是多梳抑制复合体2 (PRC2)的功能性酶成分,与长期转录抑制相关。因此,确定EZH2为与Mi-2β蛋白复合物相关的染色质调节蛋白 (图2a)。内、外源性Co-IP表明EZH2和Mi-2β存在相互作用(图2b-c),而EZH2敲减也显著上调Cxcl9和Cxcl10的水平(图2d)。 之前的研究表明, H3K27me3介导EZH2抑制ISGs的表达。体外证实EZH2沉默后,H3K27me3激活被显著抑制,且H3K27me3激活介导了由Mi-2β/EZH2复合物调控的ISG表达(图2e-g)。进一步ChIP分析证实,Mi-2β沉默后,Cxcl9和Cxcl10启动子区域的H3K27me3水平被抑制(图2h)。表明,Mi-2β和EZH2互作激活ISG转录,是由H3K27me3介导的。 图2 Mi-2β和EZH2互作激活由H3K27me3介导的ISG转录(Ref. Fig4/S6) 接下来确定Mi-2β和EZH2之间的相互作用域。截短体Co-IP实验表明,Mi-2β蛋白与EZH2的CXC结构域结合(图3a-b)。Co-IP检测EZH2的翻译后修饰,发现EZH2/Mi-2β复合物中EZH2单甲基化修饰(图3c)。研究表明EZH2甲基化使PRC2能够感知组蛋白H3,从而调节其组蛋白甲基转移酶活性。推测Mi-2β通过促进EZH2的甲基化来促进H3K27的三甲基化。质谱检测发现EZH2在K510和K735表现出单甲基化(图3d)。EZH2点突变实验表明,EZH2 K510A突变体后,H3K27的三甲基化显著降低(图3e)。表明,EZH2在K510的甲基化在H3K27甲基化的激活中起关键作用。 此外,Co-IP发现EZH2 K510甲基化是Mi-2β依赖的(图3f-h)。同时,内源性引入K510A突变体EZH2后,显著上调Cxcl9和Cxcl10(图3i)。表明,Mi-2β结合EZH2的CXC结构域,从而促进EZH2 K510甲基化,最后激活H3K27三甲基化抑制ISG转录。 另外开发了一种针对Mi-2β的Z36-MP5特异性抑制剂(图3j)。在同基因和转基因小鼠模型中,Z36-MP5通过挽救ISG表达,诱导耐药黑色素瘤对抗PD-1免疫治疗产生应答(图3k-m)。 图3 Mi-2β通过促进EZH2的K510甲基化抑制ISGs的转录(Ref. Fig4/S6) 结论:本研究通过基因筛选发现Mi-2β是调节黑色素瘤对抗肿瘤免疫应答的关键内源性效应因子,抑制Mi-2β能够在体内挽救免疫疗法的免疫应答。机制上,Mi-2β与EZH2结合,促进EZH2 K510甲基化,进而激活H3K27的三甲基化,抑制IFN-γ刺激基因(ISGs)的转录。此外,开发了针对Mi-2β的靶向抑制剂Z36-MP5,在耐药黑色素瘤模型中诱导对免疫检查点抑制剂的响应。 通讯作者简介: 崔儒涛,浙江大学/南昌大学教授,教育部实体肿瘤分子靶向医药基础研究创新中心副主任,独立PI,博士生导师。长期从事皮肤疾病和肿瘤研究,主要是黑色素瘤新靶向药物的开发研究,同时探讨色素产生和黑色素瘤发生的生物学机制。发表包括Nature和Cell等国际主流期刊通讯作者论文多篇。